From microcephaly to megalencephaly: determinants of brain size
- PMID: 30936767
- PMCID: PMC6436952
- DOI: 10.31887/DCNS.2018.20.4/gmirzaa
From microcephaly to megalencephaly: determinants of brain size
Abstract
Expansion of the human brain, and specifically the neocortex, is among the most remarkable evolutionary processes that correlates with cognitive, emotional, and social abilities. Cortical expansion is determined through a tightly orchestrated process of neural stem cell proliferation, migration, and ongoing organization, synaptogenesis, and apoptosis. Perturbations of each of these intricate steps can lead to abnormalities of brain size in humans, whether small (microcephaly) or large (megalencephaly). Abnormalities of brain growth can be clinically isolated or occur as part of complex syndromes associated with other neurodevelopmental problems (eg, epilepsy, autism, intellectual disability), brain malformations, and body growth abnormalities. Thorough review of the genetic literature reveals that human microcephaly and megalencephaly are caused by mutations of a rapidly growing number of genes linked within critical cellular pathways that impact early brain development, with important pathomechanistic links to cancer, body growth, and epilepsy. Given the rapid rate of causal gene identification for microcephaly and megalencephaly understanding the roles and interplay of these important signaling pathways is crucial to further unravel the mechanisms underlying brain growth disorders and, more fundamentally, normal brain growth and development in humans. In this review, we will (a) overview the definitions of microcephaly and megalencephaly, highlighting their classifications in clinical practice; (b) overview the most common genes and pathways underlying microcephaly and megalencephaly based on the fundamental cellular processes that are perturbed during cortical development; and (c) outline general clinical molecular diagnostic workflows for children and adults presenting with microcephaly and megalencephaly.
El crecimiento del cerebro humano, específicamente del neocórtex, está entre los procesos evolutivos más remarcables que se correlacionan con habilidades cognitivas, emocionales y sociales. El crecimiento cortical está determinado por un proceso estrictamente coordinado de la proliferación, migración, organización, sinaptogénesis y apoptosis de las células madre neurales. La alteración de cada una de estas intrincadas etapas puede llevar a anormalidades del tamaño cerebral en los humanos, sea pequeño (microcefalia) o grande (megalencefalia). Las anormalidades del crecimiento cerebral puedan estar clínicamente aisladas o constituir parte de síndromes complejos asociados con otros problemas del neurodesarrollo (como epilepsia, autismo, incapacidad intelectual), malformaciones cerebrales y anormalidades del crecimiento corporal. La revisión de la literatura genética revela que la microcefalia y la megalencefalia son causadas por mutaciones de un número rápidamente creciente de genes relacionados con las vías celulares esenciales que influyen sobre el desarrollo precoz del cerebro, con importantes mecanismos patológicos vinculados con cáncer, crecimiento corporal y epilepsia. Dada la rápida tasa de identificación de genes que causan microcefalia y megalencefalia, la comprensión del papel y de la interacción de estas importantes vías de señalización es crucial para desentrañar los mecanismos subyacentes a los trastornos del crecimiento cerebral y, más fundamentalmente, al crecimiento y desarrollo normal del cerebro en los seres humanos. En esta revisión se presenta: a) una panorámica de las definiciones de microcefalia y megalencefalia, destacando sus clasificaciones en la práctica clínica, b) una panorámica de los genes y vías más comunes que subyacen a la microcefalia y la megalencefalia basada en los procesos celulares fundamentales que están alterados durante el desarrollo cerebral y c) un resumen del plan de trabajo general para el diagnóstico clínico molecular de niños y adultos con microcefalia y megalencefalia.
L'expansion du cerveau humain, et surtout celle du néocortex, est l'un des processus les plus remarquables de l'évolution, corrélé avec les capacités cognitives, émotionnelles et sociales. L'expansion corticale est déterminée au travers d'un processus étroitement orchestré de prolifération, de migration, d'organisation, de synaptogenèse et d'apoptose des cellules souches neurales. Toute perturbation de chacune de ces étapes intriquées peut générer des anomalies de la taille du cerveau humain, qu'elle soit petite (microcéphalie) ou grande (macrocéphalie). Les anomalies de la croissance du cerveau peuvent être isolées cliniquement ou participer à des syndromes complexes associés à d'autres problèmes du neurodéveloppement (par exemple, épilepsie, autisme, déficit intellectuel), à des malformations cérébrales et à des anomalies de la croissance corporelle. Une revue de la littérature génétique montre que la microcéphalie et la macrocéphalie humaines sont dues à des mutations d'un nombre de gènes augmentant rapidement, liées à des voies cellulaires essentielles qui influent sur le développement précoce du cerveau avec des liens mécanistiques pathologiques importants aux cancers, à la croissance corporelle et a l'épilepsie. Compte tenu du taux d'identification rapide de gène causal pour la micro et la macrocéphalie, il est essentiel de comprendre les rôles et l'interaction de ces importantes voies de signalisation pour mieux découvrir les mécanismes sous-tendant les troubles de la croissance cérébrale et, plus fondamentalement, ceux de la croissance cérébrale et du développement normaux chez l'homme. Nous présentons dans cet article 1) une vue d'ensemble des définitions de la micro et de la macrocéphalie, en soulignant leurs classifications en pratique clinique 2) une vue d'ensemble des voies et des gènes les plus courants sous-tendant la micro- et la macrocéphalie d'après les processus cellulaires fondamentaux perturbés au cours du développement cortical et 3) un aperçu des plans de travail généraux du diagnostic clinique moléculaire pour les enfants et les adultes micro- et macrocéphales.
Keywords: brain size; macrocephaly; megalencephaly; microcephaly.
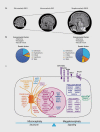
Figures
Similar articles
-
Novel loss-of-function variants in TRIO are associated with neurodevelopmental disorder: case report.BMC Med Genet. 2020 Nov 10;21(1):219. doi: 10.1186/s12881-020-01159-y. BMC Med Genet. 2020. PMID: 33167890 Free PMC article.
-
Cerebral organoids to unravel the mechanisms underlying malformations of human cortical development.Semin Cell Dev Biol. 2021 Mar;111:15-22. doi: 10.1016/j.semcdb.2020.06.001. Epub 2020 Jul 31. Semin Cell Dev Biol. 2021. PMID: 32741653 Review.
-
Proximal variants in CCND2 associated with microcephaly, short stature, and developmental delay: A case series and review of inverse brain growth phenotypes.Am J Med Genet A. 2021 Sep;185(9):2719-2738. doi: 10.1002/ajmg.a.62362. Epub 2021 Jun 4. Am J Med Genet A. 2021. PMID: 34087052 Free PMC article. Review.
-
Reciprocal Relationship between Head Size, an Autism Endophenotype, and Gene Dosage at 19p13.12 Points to AKAP8 and AKAP8L.PLoS One. 2015 Jun 15;10(6):e0129270. doi: 10.1371/journal.pone.0129270. eCollection 2015. PLoS One. 2015. PMID: 26076356 Free PMC article.
-
PIAS4 is associated with macro/microcephaly in the novel interstitial 19p13.3 microdeletion/microduplication syndrome.Eur J Hum Genet. 2015 Dec;23(12):1615-26. doi: 10.1038/ejhg.2015.51. Epub 2015 Apr 8. Eur J Hum Genet. 2015. PMID: 25853300 Free PMC article.
Cited by
-
8p23.2-pter Microdeletions: Seven New Cases Narrowing the Candidate Region and Review of the Literature.Genes (Basel). 2021 Apr 27;12(5):652. doi: 10.3390/genes12050652. Genes (Basel). 2021. PMID: 33925474 Free PMC article.
-
Pleiotropic effects of trisomy and pharmacologic modulation on structural, functional, molecular, and genetic systems in a Down syndrome mouse model.Elife. 2024 Mar 18;12:RP89763. doi: 10.7554/eLife.89763. Elife. 2024. PMID: 38497812 Free PMC article.
-
Deleterious ZNRF3 germline variants cause neurodevelopmental disorders with mirror brain phenotypes via domain-specific effects on Wnt/β-catenin signaling.Am J Hum Genet. 2024 Sep 5;111(9):1994-2011. doi: 10.1016/j.ajhg.2024.07.016. Epub 2024 Aug 20. Am J Hum Genet. 2024. PMID: 39168120 Free PMC article.
-
Genetic Analysis Algorithm for the Study of Patients with Multiple Congenital Anomalies and Isolated Congenital Heart Disease.Genes (Basel). 2022 Jun 29;13(7):1172. doi: 10.3390/genes13071172. Genes (Basel). 2022. PMID: 35885957 Free PMC article.
-
Equivocal evidence for a link between megalencephaly-related genes and primate brain size evolution.Sci Rep. 2022 Jun 28;12(1):10902. doi: 10.1038/s41598-022-12953-4. Sci Rep. 2022. PMID: 35764790 Free PMC article.
References
-
- Nellhaus G. Head circumference from birth to eighteen years. Practical composite international and interracial graphs. Pediatrics. 1968;41(1):106–114. - PubMed
-
- Roth G., Dicke U. Evolution of the brain and intelligence. Trends Cogn Sci. 2005;9(5):250–257. - PubMed
-
- Rilling JK. Comparative primate neuroimaging: insights into human brain evolution. Trends Cogn Sci. 2014;18(1):46–55. - PubMed
Publication types
MeSH terms
Grants and funding
LinkOut - more resources
Full Text Sources
